Imagerie in vitro : Services de microscopie, d'histologie et de cytométrie
Les techniques d’imagerie permettent d’observer le fonctionnement des organismes à un niveau moléculaire, cellulaire ou tissulaire par des moyens plus ou moins invasifs. De l’observation de cellules vivantes à l’aide de marqueurs moléculaires fluorescents au marquage de tissus par des anticorps spécifiques, les techniques d’imagerie permettent de visualiser la biologie d’un organisme précisément.
L’observation de la biologie de organismes se fait à plusieurs niveaux :
- Au niveau moléculaire, l’observation se fait typiquement par marquage immunologique des molécules d’intérêt, suivi d’une observation par cytométrie en flux ou par microscopie.
- Au niveau cellulaire, par marquage de différentes organelles ou par l’observation de l’état de la cellule, par exemple en cytométrie en flux.
- Au niveau tissulaire, typiquement par histologie, suite à différents marquages de structures cellulaires et moléculaires.
- Au niveau de l’organisme entier, avec des techniques de microscopie électronique après traitement de l’organisme, ou des techniques d’imagerie sur organisme vivant.
La microscopie a évolué à deux niveaux: sur le plan des grossissements, les technologies optiques pouvant aller à x 1 000 et les microscopes électroniques à transmission jusqu'à x 1 200 000; sur le plan des marquages d'intérêt, par l'utilisation de la fluorescence, les marqueurs spécifiques, la détection immunologique.
L'histologie a évolué notamment par l'acquisition de connaissances des anatomopathologistes sur l'analyse de coupes de tissus humains et autres.
La microfluidique est utilisée pour l'analyse en cytométrie en flux: ces techniques séparent les cellules pour les analyser ou les trier.
Il peut être difficile de trouver le bon laboratoire possédant l'ensemble des compétences requises pour l'imagerie des cellules, des tissus et des animaux.
Labtoo peut rechercher tout type de services d'imagerie, pour le développement de nouveaux médicaments et la mise au point de tests de diagnostic.
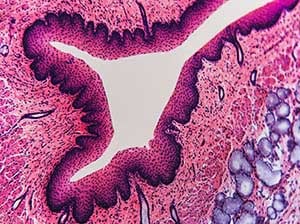
Sélectionnez votre service d'histologie, d'immuno-histochimie et d'anatomo-pathologie
L’histologie désigne l’étude microscopique de tissus et des cellules qui les composent. Pour cela, différentes techniques de marquage sont utilisées, comme la colorisation ou l’utilisation d'anticorps. L'histologie est une technique très utilisée dans le diagnostic des cellules anormales, l’anatomie pathologique ou anapath, et la distribution de marqueurs.
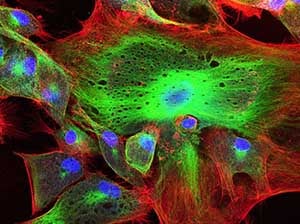
Sélectionnez votre service de microscopie confocale et électronique
La microscopie est un ensemble de techniques d'imagerie à échelle microscopique. Différentes techniques peuvent être employées telles que la microscopie confocale (microscopie à fluorescence) ou la microscopie électronique (faisceau d’électrons) à transmission et à balayage.
Sélectionnez votre service de cytométrie en flux et de tri cellulaire
La cytométrie est une technique qui permet d’étudier les cellules en suspension dans un échantillon. Elle est utilisée en immunologie car permet le marquage de nombreux biomarqueurs simultanément, plusieurs dizaines avec la cytométrie de masse. Le tri cellulaire, adapté de la cytométrie en flux, permet de récupérer les cellules en fonction de critères définis à l’avance.

Notre équipe s'occupe de la gestion de votre externalisation de R&D du début à la fin.
Réalisation d'une étude de faisabilité en recherchant l'expertise existante disponible au sein du réseau de partenaires.
Mise en place d'un protocole d'étude, devis et préparation des contrats avec les partenaires de laboratoire.
Mettre en œuvre le plan d'étude dans un calendrier, collecter tous les réactifs nécessaires et exécuter le service.
Voulez-vous plus d'informations sur les services et technologies d'imagerie in vitro ?
Les différents types de microscopes
Il existe de multiple type de microscopes, voici les différents types utilisés spécifiquement en biologie.
Stéréoscope
Le stéréoscope, également appelé microscope de dissection et stéréomicroscope, est un microscope à éclairage lumineux qui permet une vue tridimensionnelle d'un spécimen. Il utilise deux oculaires à des angles différents.
Les stéréoscopes ont une puissance inférieure à celle des microscopes composés. Les images ne sont agrandies que jusqu'à environ 100 fois, et leur application reste limitée à des contrôles de croissance en culture cellulaire, ou à de l’imagerie basique.
Composé (compound)
Un microscope composé est un instrument qui permet de visualiser des images agrandies de petits objets sur une lame de verre. Il peut atteindre des niveaux de grossissement plus élevés que les microscopes stéréo (jusqu’à 2000x) ou autres microscopes à faible puissance et réduire l'aberration chromatique. Les applications restent relativement limitées : observation directe sans système photographique couplé.
Confocal
Les microscopes confocaux sont également des microscopes utilisant la lumière, avec. Les microscopes confocaux permettent de grossir fortement les spécimens avec des images tridimensionnelles. Ils ont également des résolutions plus élevées, capables de différencier les détails jusqu'à 120 nanomètres les uns des autres. Le type de microscope confocal le plus courant est le microscope fluorescent. Ce microscope utilise une lumière intense pour exciter les molécules d'un spécimen. Ces molécules émettent de la lumière, ou fluorescence, qui est observée, ce qui permet un grossissement et une résolution plus élevés.
Microscope électronique à transmission
Le premier microscope électronique était un microscope électronique à transmission (TEM) inventé en Allemagne en 1931 par Max Knoll et Ernst Ruska. Si les microscopes à lumière peuvent grossir jusqu'à 1000x ou 2000x au mieux, alors le microscope électronique grossit les objets jusqu'à 10 000x. Un TEM fonctionne en focalisant un faisceau d'électrons à énergie unique suffisamment fort pour traverser un échantillon très mince. Les images résultantes sont ensuite visualisées par diffraction électronique ou par imagerie électronique directe.
Microscope électronique à balayage
Le microscope électronique à balayage (MEB) a été inventé au début des années 1930, et le développement du premier système commercialisé en 1965 par la Cambridge Instrument Company. Le MEB fonctionne en balayant la surface d'un échantillon avec un faisceau d'électrons. Ce faisceau crée différents signaux, des électrons secondaires, des rayons X, des photons et autres, qui aident tous à caractériser l'échantillon. Les signaux sont affichés sur un écran qui cartographie les propriétés du matériau de l'échantillon.
L’Anatomopathologie et l’histologie
L’anatomie pathologique, familièrement appelée « anapath », et officiellement dénommée anatomie et cytologie pathologiques (ACP) ou Pathologie, repose sur le diagnostic des lésions à partir de leur aspect morphologique.
Concrètement, il s’agit de poser un diagnostic à partir d’un échantillon de cellules ou de tissus. Pour cela, le médecin spécialiste va utiliser les méthodes d’histologies ou de cytologie, suivie d’une observation microscopique.
En fonction des marqueurs d’intérêt à étudier, l’histologie repose sur différentes techniques : les colorations spécifiques de composants cellulaires, l’immunologie pour détecter certaines protéines, l’hybridation in situ pour détecter des acides nucléiques.
Couramment utilisée dans le parcours de soin en anatomopathologie, notamment en cancérologie, l’histologie est à la croisée de nombreux projets de recherche : en recherche et « discovery » lors de l’analyse de biomarqueurs sur tissus, au cours d’études précliniques sur le petit animal, et tout au long des études cliniques.
Types de prestataires
Les structures académiques
La cytométrie et la microscopie nécessite un accès à des instruments de pointe, et les structures universitaires sont à même de fournir ce type de matériel et de services.
Les sociétés de service
Certaines structures spécialisées peuvent proposer des études en microscopie, notamment pour des criblages à haut contenu (HCS) ou autre projet.
Les cabinets et experts freelance
Des petits cabinets d’études proposent des services en histologie, des freelances peuvent effectuer des missions d’études anapath.
La cytométrie de masse : qu’est-ce que c’est ?
À la différence de la cytométrie en flux conventionnelle ou spectrale, qui reposent sur la fluorescence, la cytométrie de masse (CMM), qui a émergé dans les années 2010 repose sur une analyse de la masse atomique des molécules.
Les fluorophores qui étaient couplé à des fluorochromes sont désormais couplés à des isotopes de métaux non radioactifs.
Ainsi, 135 canaux de détection allant de 75 à 209 daltons sont disponibles. Chaque canal peut être attribué à un isotope, qui sera couplé à un anticorps ou une molécule ciblant les molécules d’interêt.
Les avantages de la cytométrie de masse est donc la grande disponibilité d’éléments pouvant être utilisés pour marquer les cellules : alors que la cytométrie classique est limitée à quelques marqueurs utilisés en meme temps (largement dû aux recouvrements de longueurs d’ondes des fluorophores et au bruit de fond des échantillons), la CMM se libère de ces contraintes. Cela permet également d’étudier des événements rares et de normaliser les analyses à partir de standards quantifiables.
Enfin, la CMM possède un avantage de taille : la préparation des échantillons et la planification des études se fait de façon similaire (ou même parfois simplifiée !) par rapport à la cytométrie conventionelle. Cela facilite le transfert de méthode et de ne pas devoir repartir d’une feuille blanche.

